При входе на сайт вы даете согласие на обработку персональных данных в соответствии с пользовательским соглашением
Внешний вид упаковки может отличаться от фотографии












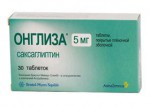
Онглиза®
Действующее вещество
Саксаглиптин*(Saxagliptinum)
Фармакологическая группа
Гипогликемические синтетические и другие средства
Состав
Таблетки, покрытые пленочной оболочкой 1 табл.
активное вещество:
саксаглиптин (в виде саксаглиптина гидрохлорида) 2,5 мг
5 мг
вспомогательные вещества: лактозы моногидрат — 99 мг*; МКЦ — 90 мг; кроскармеллоза натрия — 10 мг; магния стеарат — 1 мг**; 1М раствор хлористоводородной кислоты*** — q.s.; Opadry II белый — 26 мг (спирт поливиниловый — 40%, титана диоксид — 25%, макрогол (ПЭГ 3350) — 20,2%, тальк — 14,8%); Opadry II желтый — 7 мг (спирт поливиниловый — 40%, титана диоксид — 24,25%, макрогол (ПЭГ 3350) — 20,2%, тальк — 14,8%, краситель оксид железа желтый (E172) — 0,75%) (для дозировки 2,5 мг); Opadry II розовый — 7 мг (спирт поливиниловый — 40%, титана диоксид — 24,25%, макрогол (ПЭГ 3350) — 20,2%, тальк — 14,8%, краситель оксид железа красный (E172) — 0,75%) (для дозировки 5 мг); чернила Opacode синий — q.s.
* Количество лактозы может варьировать в зависимости от используемого количества магния стеарата.
** Количество магния стеарата может варьировать в пределах 0,5–2 мг, оптимальное количество 1 мг.
*** В случае необходимости для доведения рН может использоваться 1М натрия гидроксид.
состав чернил Opacode синий: шеллак 45% в спирте этиловом — 55,4%; FD&C Blue#2/индиго карминовый алюминиевый пигмент (E132) — 16%; спирт н-бутиловый — 15%; пропиленгликоль — 10,5%; спирт изопропиловый — 3%; 28% аммония гидроксид — 0,1%
очень небольшие количества шеллака и FD&C Blue#2/индиго карминового алюминиевого пигмента остаются на таблетках при нанесении маркировки, растворители, входящие в состав чернил, удаляются в процессе производства
Описание лекарственной формы
Таблетки, покрытые пленочной оболочкой, 2,5 мг: круглые двояковыпуклые, покрытые пленочной оболочкой от бледно-желтого до светло-желтого цвета, с надписями «2,5» на одной стороне и «4214» — на другой стороне, нанесенными синим красителем.
Таблетки, покрытые пленочной оболочкой, 5 мг: круглые двояковыпуклые, покрытые пленочной оболочкой розового цвета, с надписями «5» на одной стороне и «4215» — на другой стороне, нанесенными синим красителем.
Фармакологическое действие
Фармакологическое действие - гипогликемическое.
Фармакодинамика
Саксаглиптин — мощный селективный обратимый конкурентный ингибитор дипептидилпептидазы-4 (ДПП-4). У пациентов с сахарным диабетом типа 2 (СД2) прием саксаглиптина приводит к подавлению активности фермента ДПП-4 в течение 24 ч. После приема глюкозы внутрь ингибирование ДПП-4 приводит к 2–3-кратному увеличению концентрации глюкагоноподобного пептида-1 (ГПП-1) и глюкозозависимого инсулинотропного полипептида (ГИП), уменьшению концентрации глюкагона и усилению глюкозозависимой ответной реакции бета-клеток, что приводит к повышению концентрации инсулина и С-пептида. Высвобождение инсулина бета-клетками поджелудочной железы и снижение высвобождения глюкагона из панкреатических альфа-клеток приводит к снижению гликемии натощак и постпрандиальной гликемии.
Эффективность и безопасность применения саксаглиптина при приеме в дозах 2,5, 5 и 10 мг 1 раз в сутки изучены в шести двойных слепых плацебо-контролируемых исследованиях с участием 4148 пациентов с СД2. Прием препарата сопровождался статистически значимым улучшением показателей гликозилированного гемоглобина (HbA1c), глюкозы плазмы крови натощак (ГПН) и постпрандиальной глюкозы (ППГ) плазмы крови по сравнению с контролем.
Саксаглиптин назначался в виде монотерапии или комбинированной терапии. Комбинированная терапия саксаглиптином назначалась дополнительно пациентам, некомпенсированным при проведении монотерапии метформином, глибенкламидом, тиазолидиндионами или инсулином, или в качестве стартовой комбинации с метформином пациентам, некомпенсированным на диете и физических упражнениях. При приеме саксаглиптина в дозе 5 мг снижение HbA1с было отмечено через 4 нед и ГПН — через 2 нед.
В группе пациентов, получавших саксаглиптин в комбинации с метформином, глибенкламидом или тиазолидиндионами, снижение HbA1с также отмечалось через 4 нед и ГПН — через 2 нед.
В исследовании комбинированной терапии саксаглиптином и инсулином (в т.ч. в комбинации с метформином) с участием 455 пациентов с СД2 продемонстрировано существенное снижение HbA1с и ППГ по сравнению с плацебо.
Влияние саксаглиптина на липидный профиль сходно с таковым плацебо. На фоне терапии саксаглиптином не отмечено увеличение массы тела.
В прямом сравнительном исследовании с участием 858 пациентов с СД2 добавление препарата Онглиза® 5 мг к метформину по сравнению с добавлением глипизида к метформину продемонстрировало сравнимое снижение HbA1c, однако было ассоциировано с достоверно меньшим числом эпизодов гипогликемии — 3% случаев по сравнению с 36,3% при добавлении глипизида, а также отсутствием увеличения массы тела у пациентов, получающих терапию саксаглиптином (−1,1 кг от исходного уровня в группе саксаглиптина, +1,1 кг в группе глипизида).
Фармакокинетика
У пациентов с СД2 и здоровых добровольцев отмечены сходные параметры фармакокинетики саксаглиптина и его основного метаболита. Саксаглиптин быстро абсорбируется после приема внутрь натощак с достижением Cmax саксаглиптина и основного метаболита в плазме в течение 2 и 4 ч соответственно. При увеличении дозы саксаглиптина было отмечено пропорциональное увеличение Cmax и величины AUC саксаглиптина и его основного метаболита. После однократного приема саксаглиптина внутрь в дозе 5 мг здоровыми добровольцами средние значения AUC саксаглиптина и его основного метаболита составили 78 и 214 нг·ч/мл, а значения Cmax в плазме — 24 и 47 нг/мл соответственно.
Средняя продолжительность конечного T1/2 саксаглиптина и его основного метаболита составила 2,5 и 3,1 ч соответственно, а средняя величина T1/2 ингибирования ДПП-4 плазмы — 27 ч. Ингибирование активности ДПП-4 в плазме в течение по крайней мере 24 ч после приема саксаглиптина обусловлено его высоким сродством к ДПП-4 и длительным связыванием с ним. Заметной кумуляции саксаглиптина и его основного метаболита при длительном приеме препарата 1 раз в день не наблюдалось. Не было выявлено зависимости клиренса саксаглиптина и его основного метаболита от дозы препарата и длительности терапии при приеме саксаглиптина 1 раз в день в дозах от 2,5 до 400 мг на протяжении 14 дней.
Всасывание
После приема внутрь всасывается не менее 75% принятой дозы саксаглиптина. Прием пищи не оказывал существенное влияние на фармакокинетику саксаглиптина у здоровых добровольцев. Прием пищи с высоким содержанием жиров не оказывал влияние на Cmax саксаглиптина, тогда как AUC увеличивалась на 27% по сравнению с приемом натощак. Tmax для саксаглиптина увеличивалось приблизительно на 0,5 ч при приеме препарата вместе с пищей по сравнению с приемом натощак. Однако эти изменения не являются клинически значимыми.
Распределение
Связывание саксаглиптина и его основного метаболита с белками сыворотки крови незначительно, поэтому можно предположить, что распределение саксаглиптина при изменениях белкового состава сыворотки крови, отмечающихся при печеночной или почечной недостаточности, не будет подвержено значительным изменениям.
Метаболизм
Саксаглиптин метаболизируется главным образом при участии изоферментов цитохрома Р450 CYP3A4/5 с образованием активного основного метаболита, ингибирующее действие которого в отношении ДПП-4 выражено в 2 раза слабее, чем у саксаглиптина.
Выведение
Саксаглиптин выводится с мочой и желчью. После однократного приема дозы 50 мг меченного 14C-саксаглиптина 24% дозы выводились почками в виде неизмененного саксаглиптина и 36% — в виде основного метаболита саксаглиптина. Общая радиоактивность, обнаруженная в моче, соответствовала 75% принятой дозы препарата. Средний почечный клиренс саксаглиптина составил около 230 мл/мин, среднее значение клубочковой фильтрации — примерно 120 мл/мин. Для основного метаболита почечный клиренс был сопоставим со средними значениями клубочковой фильтрации.
Около 22% общей радиоактивности было обнаружено в фекалиях.
Фармакокинетика в особых клинических ситуациях
Нарушение функции почек. У пациентов с легкой степенью почечной недостаточности величина AUC саксаглиптина и его основного метаболита были соответственно в 1,2 и 1,7 раза выше, чем аналогичные показатели у лиц с нормальной функцией почек. Данное увеличение значений AUC не является клинически значимым, поэтому коррекция дозы не требуется.
У пациентов с почечной недостаточностью умеренной и тяжелой степени, а также у пациентов на гемодиализе величины AUC саксаглиптина и его основного метаболита были соответственно в 2,1 и 4,5 раза выше, чем аналогичные показатели у лиц с нормальной функцией почек. Для пациентов с умеренным и тяжелым нарушением функции почек, а также для пациентов на гемодиализе доза саксаглиптина должна составлять 2,5 мг 1 раз в сутки (см. «Способ применения и дозы», «Особые указания»).
Нарушение функции печени. У пациентов с легким, умеренным и тяжелым нарушением функции печени не было выявлено клинически значимых изменений параметров фармакокинетики саксаглиптина, поэтому коррекция дозы для таких пациентов не требуется.
Пациенты пожилого возраста. У пациентов 65–80 лет не было выявлено клинически значимых различий параметров фармакокинетики саксаглиптина по сравнению с пациентами более молодого возраста (18–40 лет), поэтому коррекция дозы у пожилых пациентов не требуется. Однако следует учитывать, что у этой категории пациентов более вероятно снижение функции почек (см. «Способ применения и дозы», «Особые указания»).
Показания
Сахарный диабет типа 2 в дополнение к диете и физическим упражнениям для улучшения гликемического контроля в качестве монотерапии; стартовой комбинированной терапии с метформином; добавления к монотерапии метформином, тиазолидиндионами, производными сульфонилмочевины, инсулином (в т.ч. в комбинации с метформином) при отсутствии адекватного гликемического контроля на данной терапии (см. «Противопоказания», С осторожностью и «Особые указания»).
Противопоказания
повышенная индивидуальная чувствительность к любому компоненту препарата;
серьезные реакции повышенной чувствительности (анафилаксия или ангионевротический отек) к ингибиторам ДПП-4;
сахарный диабет типа 1 (применение не изучено);
диабетический кетоацидоз;
врожденная непереносимость галактозы, лактазная недостаточность и глюкозо-галактозная мальабсорбция;
беременность;
лактация;
возраст до 18 лет (безопасность и эффективность не изучены).
С осторожностью: почечная недостаточность умеренной и тяжелой степени; пожилые пациенты; совместное применение с производными сульфонилмочевины или инсулином; пациенты с панкреатитом в анамнезе (связь между приемом препарата и повышенным риском развития панкреатита не установлена).
Применение при беременности и кормлении грудью
В связи с тем, что применение саксаглиптина в период беременности не изучено, не следует назначать препарат в период беременности.
Неизвестно, проникает ли саксаглиптин в грудное молоко. В связи с тем, что не исключена возможность проникновения саксаглиптина в грудное молоко, следует прекратить грудное вскармливание на период лечения саксаглиптином или отменить терапию, учитывая соотношение риска для ребенка и пользы для матери.
Побочные действия
В таблице приведены побочные эффекты, выявленные у пациентов с СД2 при приеме препарата Онглиза® в дозе 5 мг в ходе клинических исследований. Общая частота нежелательных явлений при приеме препарата Онглиза® в дозе 5 мг в режиме монотерапии и в режиме добавления к терапии метформином, тиазолидиндионом или глибенкламидом была сопоставима с таковой в группе плацебо.
Шкала частоты побочных реакций: очень часто (≥1/10); часто (≥1/100, но <1/10); нечасто (≥1/1000, но <1/100); редко (≥1/10000, но <1/1000); очень редко (<1/10000).
Таблица
Побочные эффекты по данным объединенного анализа 5 плацебо-контролируемых клинических исследований препарата Онглиза®
Побочные эффекты Частота побочных эффектов
Инфекции и инвазии:
Инфекции верхних дыхательных путей Часто
Инфекции мочевыводящих путей Часто
Гастроэнтерит Часто
Синусит Часто
Со стороны ЖКТ:
Рвота Часто
Со стороны нервной системы:
Головная боль Часто
Частота реакций гиперчувствительности, отмеченных к 24-й неделе терапии, составила 1,5% у пациентов, получавших препарат Онглиза® 5 мг, и 0,4% у пациентов, получавших плацебо. Реакции гиперчувствительности, возникшие у пациентов, принимавших препарат Онглиза®, не требовали госпитализации и были расценены лечащими врачами как не представлявшие угрозу жизни.
Побочные эффекты препарата Онглиза® при комбинированной терапии
В исследовании по комбинированному применению саксаглиптина и глибенкламида частота подтвержденных эпизодов гипогликемии в группе саксаглиптина 5 мг (0,8%) и плацебо (0,7%) статистически не различалась. Частота подтвержденных эпизодов гипогликемии у пациентов, получавших препарат Онглиза® 5 мг в ходе двух исследований саксаглиптина в режиме монотерапии, исследовании по комбинированной терапии саксаглиптином и метформином, а также в исследовании по комбинированному применению саксаглиптина и тиазолидиндионов, была сопоставима с таковой на фоне плацебо.
В исследовании по применению комбинации саксаглиптина и инсулина общая частота развития гипогликемии составила 18,4% в группе саксаглиптина 5 мг и 19,9% в группе плацебо.
В исследовании по применению саксаглиптина совместно с тиазолидиндионами частота периферических отеков была выше в группе саксаглиптина 5 мг по сравнению с группой плацебо (8,1 и 4,3% соответственно). Периферические отеки были слабо или умеренно выраженными и не приводили к прекращению лечения. Частота периферических отеков у пациентов, принимавших препарат Онглиза® в дозе 5 мг в ходе клинических исследований монотерапии саксаглиптином и комбинированной терапии с метформином или глибенкламидом, была сопоставима с таковой на фоне плацебо (1,7 и 2,4% соответственно).
При стартовой комбинированной терапии саксаглиптином в дозе 5 мг и метформином часто отмечались случаи назофарингита и головной боли. Частота назофарингита была выше на фоне комбинированной терапии (6,9%) по сравнению с монотерапией саксаглиптином 10 мг (4,2%) и метформином (4%). Головная боль была чаще в группе пациентов на комбинированной терапии метформином и саксаглиптином 5 мг (7,5%) по сравнению с группами монотерапии саксаглиптином 10 мг (6,3%) и метформином (5,2%).
Постмаркетинговое применение
В ходе постмаркетингового применения саксаглиптина зарегистрированы следующие побочные эффекты: острый панкреатит и реакции гиперчувствительности, включая анафилаксию, ангионевротический отек, сыпь и крапивницу. Достоверно оценить частоту развития данных явлений невозможно, поскольку сообщения получены спонтанно, от популяции неустановленного размера (см. «Противопоказания», «Особые указания»).
Лабораторные исследования
В клинических исследованиях частота изменений лабораторных показателей при приеме саксаглиптина в дозе 5 мг и плацебо была сопоставимой. Отмечалось небольшое снижение числа лимфоцитов, при этом среднее абсолютное число лимфоцитов оставалось стабильным и в пределах нормальных значений при ежедневном приеме саксаглиптина продолжительностью до 102 нед. Уменьшение количества лимфоцитов не сопровождалось клинически значимыми нежелательными реакциями. Клиническое значение уменьшения числа лимфоцитов на фоне терапии саксаглиптином неизвестно.
Взаимодействие
Анализ данных клинических исследований позволяет предполагать, что риск клинически значимых взаимодействий саксаглиптина с другими ЛС при их совместном применении невелик.
Метаболизм саксаглиптина преимущественно опосредован системой изоферментов цитохрома Р450 CYP3A4/5. В исследованиях in vitro было показано, что саксаглиптин и его основной метаболит не ингибируют изоферменты CYP1A2, 2А6, 2В6, 2С9, 2С19, 2D6, 2Е1 и 3А4 и не индуцируют изоферменты CYP1A2, 2В6, 2С9 и 3А4.
В исследованиях с участием здоровых добровольцев фармакокинетические показатели саксаглиптина и его основного метаболита значимо не изменялись под влиянием метформина, глибенкламида, пиоглитазона, дигоксина, симвастатина, дилтиазема, кетоконазола, омепразола, комбинации алюминия гидроксида, магния гидроксида и симетикона, а также фамотидина. Саксаглиптин значимо не изменяет фармакокинетические показатели метформина, глибенкламида, пиоглитазона, дигоксина, симвастатина, дилтиазема, кетоконазола или перорального комбинированного (эстроген+гестаген) контрацептивного средства.
Влияние индукторов изоферментов CYP3A4/5 на фармакокинетику саксаглиптина не изучено. Однако совместное применение саксаглиптина и индукторов изоферментов CYP3A4/5, таких как карбамазепин, дексаметазон, фенобарбитал, фенитоин и рифампицин, может приводить к уменьшению концентрации саксаглиптина в плазме и увеличению концентрации его основного метаболита.
Изучение влияния курения, диетического питания, приема растительных препаратов и употребления алкоголя на терапию саксаглиптином не проводилось.
Способ применения и дозы
Внутрь, независимо от приема пищи.
Монотерапия: рекомендуемая доза саксаглиптина составляет 5 мг 1 раз в сутки.
Комбинированная терапия: рекомендуемая доза саксаглиптина составляет 5 мг 1 раз в сутки в комбинации с метформином, тиазолидиндионами, производными сульфонилмочевины или инсулином (в т.ч. в комбинации с метформином).
При стартовой комбинированной терапии с метформином рекомендуемая доза саксаглиптина составляет 5 мг 1 раз в сутки, начальная доза метформина — 500 мг/сут. В случае неадекватного ответа доза метформина может быть увеличена.
При пропуске приема препарата Онглиза® пропущенную таблетку следует принять сразу, как только пациент об этом вспомнит, однако не следует принимать двойную дозу препарата в течение одних суток.
Применение у особых групп пациентов
Пациенты с нарушением функции почек. Для пациентов с почечной недостаточностью легкой степени (Cl креатинина >50 мл/мин) коррекция дозы не требуется. Для пациентов с умеренной или тяжелой почечной недостаточностью (Cl креатинина ≤50 мл/мин), а также для пациентов, находящихся на гемодиализе, рекомендуемая доза препарата Онглиза® составляет 2,5 мг 1 раз в сутки. Препарат следует принимать по окончании сеанса гемодиализа.
Применение саксаглиптина у пациентов на перитонеальном диализе не изучено.
Перед началом терапии саксаглиптином и в процессе лечения рекомендуется проводить оценку функции почек.
Пациенты с нарушением функции печени. При нарушении функции печени легкой, умеренной и тяжелой степени коррекция дозы не требуется.
Пациенты пожилого возраста. Коррекция дозы у пожилых пациентов не требуется. Однако при выборе дозы следует учитывать, что у этой категории пациентов более вероятно снижение функции почек.
Дети. Безопасность и эффективность применения препарата у пациентов младше 18 лет не изучалась.
Одновременное применение с мощными ингибиторами CYP3A4/5
При одновременном применении с мощными ингибиторами CYP3A4/5, такими как кетоконазол, атазанавир, кларитромицин, индинавир, итраконазол, нефазодон, нелфинавир, ритонавир, саквинавир и телитромицин, рекомендуемая доза препарата Онглиза® составляет 2,5 мг 1 раз в сутки.
Передозировка
Симптомов интоксикации не описано при длительном приеме препарата в дозах, до 80 раз превышающих рекомендованные.
Лечение: в случае передозировки следует применять симптоматическую терапию. Саксаглиптин и его основной метаболит выводятся из организма при помощи гемодиализа (скорость выведения: 23% дозы за 4 ч).
Особые указания
Применение препарата Онглиза® в составе тройной терапии с метформином и тиазолидиндионами или метформином и производными сульфонилмочевины не изучалось.
Пациенты с нарушением функции почек. Рекомендуется коррекция дозы для пациентов с умеренной и тяжелой почечной недостаточностью, а также для пациентов на гемодиализе. Перед началом терапии и периодически в процессе лечения препаратом рекомендуется проводить оценку функции почек.
Применение в комбинации с препаратами, которые могут вызвать гипогликемию. Производные сульфонилмочевины могут вызвать гипогликемию, поэтому для уменьшения риска гипогликемии при одновременном применении с препаратом Онглиза® может потребоваться снижение дозы производных сульфонилмочевины или инсулина.
Реакции гиперчувствительности. В ходе постмаркетингового применения саксаглиптина отмечены серьезные реакции гиперчувствительности, включая анафилаксию и ангионевротический отек. При развитии серьезной реакции гиперчувствительности следует прекратить применение препарата, оценить другие возможные причины развития явления и назначить альтернативную терапию сахарного диабета (см. «Противопоказания», «Побочные действия»).
Панкреатит. В рамках постмаркетингового применения препарата получены спонтанные сообщения о случаях острого панкреатита. Пациенты, принимающие препарат Онглиза®, должны быть проинформированы о характерном симптоме острого панкреатита — продолжительная, интенсивная боль в области живота. При подозрении на развитие панкреатита следует прекратить прием препарата Онглиза® (см. «Противопоказания», С осторожностью, «Побочные действия»).
Пациенты пожилого возраста. По данным клинических исследований, показатели эффективности и безопасности у пациентов в возрасте 65 лет и старше не отличались от аналогичных показателей у пациентов более молодого возраста. Однако нельзя исключить повышенную индивидуальную чувствительность к саксаглиптину у некоторых пациентов пожилого возраста. Саксаглиптин и его основной метаболит частично выводятся почками, поэтому необходимо учитывать, что у пациентов пожилого возраста более вероятно снижение функции почек.
Препарат Онглиза® содержит лактозу. Пациенты с врожденной непереносимостью галактозы, лактазной недостаточностью и глюкозо-галактозной мальабсорбцией не должны принимать этот препарат.
Влияние на способность управлять автомобилем или выполнять работы, требующие повышенной скорости физических и психических реакций. Исследования по изучению влияния саксаглиптина на способность к вождению автотранспорта и управлению механизмами не проводились. Следует учитывать, что саксаглиптин может вызывать головокружение.
Условия отпуска
По рецепту.
Условия хранения
При температуре не выше 30 °C.
Хранить в недоступном для детей месте.